SISSEJUHATUS
Ravijuhend sisaldab suuniseid kõikidele arstidele, õdedele ja ämmaemandatele, kes puutuvad oma töös kokku 40–65-aastaste täiskasvanute tervise jälgimise ja haiguste ennetusega.
-
südame-veresoonkonnahaigused,
-
2. tüüpi diabeet,
-
eesnäärmevähk,
-
glaukoom,
-
osteoporoos,
-
D-hüpovitaminoosist tingitud haigestumine,
-
depressioon ja ärevushäire.
-
tubaka- ja nikotiinitoodete tarvitamine,
-
narkootiliste ainete tarvitamine,
-
alkoholitarvitamine,
-
ebapiisav kehaline aktiivsus,
-
ebatervislik toitumine.
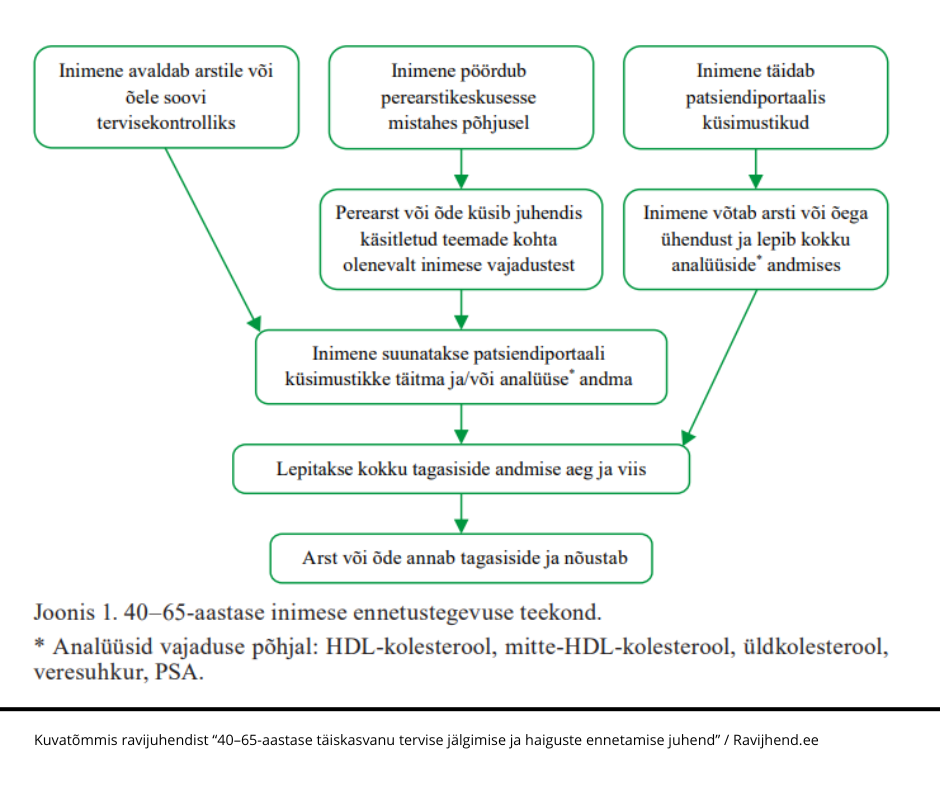
Ennetustegevuseni võib jõuda järgmistel viisidel:
- inimene pöördub arsti või õe poole sooviga tulla tervisekontrolli,
- inimene pöördub mistahes põhjusel perearstikeskusesse ja ennetusteema algatab arst või õde,
- inimene täidab ise enda kohta ennetusküsimustikud, misjärel võtab ühendust arsti või õega.
Ravijuhend ei asenda tervishoiutöötaja individuaalset vastutust teha õigeid (ravi)otsuseid konkreetsest inimesest lähtudes.
Täiskasvanute tervise jälgimise ja haiguste ennetamise juhend sai alguse tervisetehnoloogia hindamise raporti „Tervisekontrollid südame-veresoonkonnahaiguste ja diabeedi ennetuseks, TTH56“ koostamisest ( 1 ).
Ravijuhendi soovitused koos tõenduse lühikokkuvõttega
Eestis on südame-veresoonkonnahaiguste (SVH) riski hindamiseks olnud siiani kasutusel riskiskoor SCORE. 2021. aastal avaldas Euroopa Kardioloogide Selts uue SVH-de ennetamise ravijuhendi (3), milles soovitatakse kasutada tervetel, varasema SVH ja diabeedi diagnoosita 40–69-aastastel inimestel SVH riski hindamiseks riskiskoori SCORE2.
SCORE-i abil saab välja arvestada kümne aasta jooksul surmaga lõppeva SVH kujunemise riski, kuid riskiskooris SCORE2 võetakse arvesse ka surmaga mittelõppevate SVH-de haiguskoormust, sest nende osatähtsus on aastatega aina kasvanud. Lisaks nüüdisajastati SCORE2 väljatöötamisel riskiskoori sobivust tänapäevaste SVH-de avaldumusega, et see vastaks paremini Euroopa praegusele elanikkonnale. Seetõttu jagatakse SCORE2-s riigid nelja riskirühma: väikese, keskmise, suure ja väga suure SVH riskiga riigid.
Eesti kuulub suure riskiga riikide hulka. Kui SCORE-is arvestatakse üldkolesterooli sisaldust, siis SCORE2 puhul vaadatakse mitte-HDL-kolesterooli sisaldust. Mõlemas riskiskooris võetakse lisaks arvesse sugu, vanust, suitsetamist ja süstoolset vererõhku.
Südame-veresoonkonnahaigused on kõige sagedam surmapõhjus nii meeste kui ka naiste seas kogu maailmas. Teada on nii põhjuslik kui ka kumulatiivne seos LDL-kolesterooli suurenenud väärtuse ja aterosklerootilise südamehaiguse vahel. On leitud, et kui LDL-kolesterooli sisaldus intensiivselt väheneb, aitab see omakorda vähendada südame-veresoonkonna sündmusi (6, 7, 8). Kolesteroolisisaldust vähendavatest ravimitest on esmavalikuks statiinid (9).
2. Riskiskoori SCORE2 hinnangu alusel väga suure südame-veresoonkonnahaiguste riskiga 40–65-aastasele inimesele
määrake statiinravi.Tugev positiivne soovitus, mõõdukas tõendatuse aste
3. Riskiskoori SCORE2 hinnangu alusel suure südameveresoonkonnahaiguste riskiga 40–65-aastasel inimesel hinnake enne statiinraviga alustamist eluviisimuutuste vajadust ning vajaduse korral nõustage teda.
Praktiline soovitus
4. Riskiskoori SCORE2 hinnangu alusel suure südameveresoonkonnahaiguste riskiga 40–65-aastasele inimestele kaaluge statiinravi määramist.
Nõrk positiivne soovitus, mõõdukas tõendatuse aste
5. Riskiskoori SCORE2 hinnangu alusel suure või väga suure südame-veresoonkonnahaiguste riskiga 40–65-aastasel inimesel eelistage suure intensiivsusega statiine.
Praktiline soovitus
6. Väga suure südame-veresoonkonnahaiguste riskiga 40–65-aastase inimese LDL-kolesterooli ravieesmärk on ˂ 1,4 mmol/L ja LDL-kolesterooli sisalduse vähenemine 50% või enam algsest LDL-kolesterooli väärtusest.
Praktiline soovitus
7. Suure südame-veresoonkonnahaiguste riskiga 40–65-aastase inimese LDL-kolesterooli ravieesmärk on ˂ 1,8 mmol/L ja LDL-kolesterooli sisalduse vähenemine 50% või enam algsest LDL-kolesterooli väärtusest.
Praktiline soovitus
Olemasolev tõendusmaterjal suure südame-veresoonkonnahaiguste riskiga inimeste statiinravi vajaduse ja ravieesmärkide kohta pärineb ühest metanalüüsist
(10), kahest süstemaatilisest ülevaatest (9, 11) ja juhuslikustatud kontrolluuringust (8, 12, 13) ning peamiselt Euroopa Kardioloogide Seltsi (ESC) ja Euroopa
Ateroskleroosi Ühingu (EAS) 2019. aasta (6) ja ESC 2021. aasta (3) ravijuhenditest.
Statiinravi vajadus
2020. aastal avaldatud metaanalüüsis, kuhu kaasati 52 uuringut üle 327 000 patsiendiga, näidati, et statiinraviga LDL-kolesterooli sisalduse alandamine 1
mmol/L võrra vähendas oluliste kardiovaskulaarsete tüsistuste riski 19% võrra (14).
Cochrane’i analüüsi tulemuste kohaselt vähendas statiinravi esmase ennetusena nii üldist suremust, koronaarhaiguse tüsistuste, südame-veresoonkonna sündmuste ja insuldi riski kui ka revaskulariseerimise vajadust (9). Sarnased tulemused saadi ka 2016. aastal avaldatud 19 uuringut kaasanud metaanalüüsis (11). Samuti leiti, et statiinravi saajate hulgas oli müokardiinfarkti tõenäosus väiksem.
Sandwichi ja Forgeti 2021. aastal avaldatud metaanalüüsis (10) jaotati uuringud patsiendipõhiselt kahte rühma: esimesse rühma kuulusid uuringud, kus osa
uuritavaid olid kaasuvate haigusteta, ja teise rühma uuringud, kus uuritavad olid kaasuvate haigustega (enamasti hüpertensioon ja diabeet). Metaanalüüsis
oli eraldi rühmana plaanis hinnata ka ainult ilma kaasuvate haigusteta (v.a düslipideemia) patsiente hõlmanud uuringuid, kuid selliseid uuringuid ei leitud.
Kõigis alarühmades ja kõigi tulemusnäitajate puhul vähenes risk statiinravi saanute rühmas. Alarühmade võrdluses leiti erinevus vaid südame-veresoonkonna
sündmuste tekke tulemusnäitaja puhul: rühmas, kus oli mh kaasuvate haigusteta uuritavaid, esines südame-veresoonkonna sündmusi 12% vähem.
Ravieesmärgid
Teada on nii põhjuslik kui ka kumulatiivne seos LDL-kolesterooli suurenenud väärtuse ja aterosklerootilise südamehaiguse vahel. On leitud, et LDL-kolesterooli sisalduse intensiivne vähenemine vähendab ka südame-veresoonkonna sündmusi (6, 7). Sekkumise valik peaks põhinema kardiovaskulaarsel riskil ja LDL-kolesterooli väärtusel.
Paljudes metaanalüüsides ja juhuslikustatud uuringutes on näidatud, et suhtelise riski vähenemine on proportsionaalne LDL-kolesterooli absoluutväärtuse vähendamisega ning LDL-kolesterooli absoluutväärtuse vähenemine sõltub ainult LDL-kolesterooli algsest sisaldusest. Mida kõrgem on algne LDL-kolesterooli väärtus, seda enam väheneb absoluutne risk (6, 8, 12, 13, 15, 16). Pole kindlaks tehtud, millisest LDL-kolesterooli väärtusest madalam sisaldus tooks kaasa negatiivseid tagajärgi (6, 8).
Käsitlusala koostades ei püstitanud töörühm küsimust ravieesmärgi kohta, kuid töö käigus selgus, et kui antakse soovitus määrata statiine, peaks käsitlema
ka ravieesmärke. Eeskujuks võeti ESC 2021. aasta ravijuhend (3), mille põhjal otsustati anda praktilised soovitused. LDL-kolesterooli eesmärkväärtuste algoritm on esitatud lisas 1.
Ravijuhendi „Täiskasvanute kõrgvererõhktõve käsitlus esmatasandil“ põhjal on alla 65-aastastel inimestel soovitatav saavutada vererõhuväärtus 120–130/80
mmHg (süstoolne vererõhk mitte alla 120 mmHg) (17).
Statiini valik
Vere kolesteroolisisaldust vähendavatest ravimitest on esmavalikuks statiinid (9).
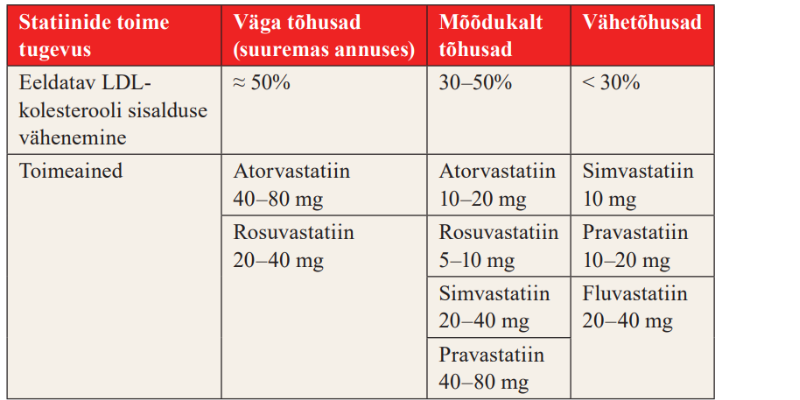
Statiinid jaotatakse nende võime järgi vähendada LDL-kolesterooli sisaldust veres (vt tabel 1) (15). Arvestades ravieesmärke, tuleks eelistada suure intensiivsusega statiine maksimaalses talutavas annuses (8, 18, 19).
Tabel 1. Statiinid toime tugevuse ja vere LDL-kolesterooli sisalduse vähendamise tõhususe järgi
Töörühm võttis soovituste sõnastamisel arvesse, et statiinide laialdasema kasutamisega kõigi kõrge või väga kõrge SVH riskiga inimeste puhul kaasneb
kulu, kuid see on pigem tagasihoidlik. Saadav kasu südame-veresoonkonna sündmuste vähenemisest ning töövõime ja elukvaliteedi paranemisest kaalub
kulu tõenäoliselt üles.
Käsitlusala koostades ei püstitanud töörühm küsimust statiinide valiku kohta, kuid töö käigus selgus, et kui antakse soovitus statiine määrata, peaks käsitlema ka seda, milliste statiinidega ravida. Eeskujuks võeti 2021. aastal ilmunud Euroopa Kardioloogide Seltsi kardiovaskulaarsete haiguste ennetamise ravijuhend (3), mille põhjal otsustati anda praktiline soovitus.
SCORE2 algoritm on esitatud lisas 2. Algoritm põhineb Euroopa Kardioloogide Seltsi kardiovaskulaarsete haiguste ennetamise 2021. aasta juhendil (3). Algoritmis on kasutatud mitte-HDL-kolesterooli, mis on arvutuslik parameeter, mille väljastab labor automaatselt või mille arvutamiseks lahutatakse üldkolesterooli väärtusest HDL-kolesterooli väärtus.
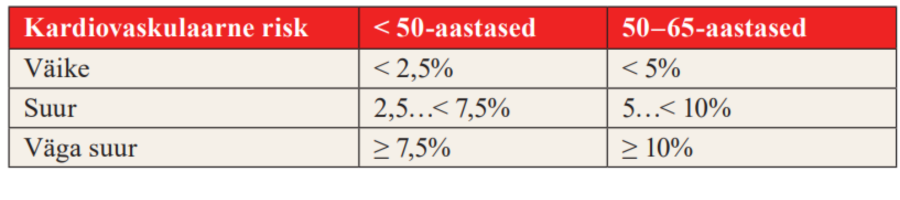
Tabel 2. SCORE2-l põhinevad südame-veresoonkonnahaiguste 10 aasta riski kategooriad
Vaata lähemalt kolmanda kliinilise küsimuse TõKo ja SoKo tabelit.
Tervise Arengu Instituudi andmetel diagnoositakse Eestis aastas umbes 4500 esmast diabeedijuhtu, millest enamuse moodustab 2. tüüpi diabeet. On iseloomulik, et 2. tüüpi diabeedi esmajuhtudest diagnoositakse 90% vähemalt 45-aastastel inimestel.
Hinnangute kohaselt on Eestis diagnoositud diabeet umbes 70 000 inimesel, kuid arvatakse, et umbes sama palju inimesi põeb diabeeti enese teadmata. Võimalike diabeedijuhtumite avastamiseks on kasutusel mitmesuguseid analüüse: näiteks määratakse paastuglükoosi, glükohemoglobiini (HbA1c) või
tehakse glükoositaluvuse proov (GTT). (20)
40–65-aastasele 2. tüüpi diabeedi riskiga inimesele võite määrata paastuglükoosi või glükohemoglobiini analüüsi haiguse varaseks avastamiseks.
Nõrk positiivne soovitus, madal tõendatuse aste
Tõendus pärineb kuuest kokkuvõttes madala kvaliteediga metanalüüsist (21, 22, 23, 24, 25, 26) ja ühest süstemaatilisest ülevaatest (27). Diabeedi sõeluuringus tehakse nii glükohemoglobiini kui ka paastuglükoosi analüüsid, mis on vähese tundlikkuse ja üsna hea spetsiifilisusega. Vähene tundlikkus tähendab, et analüüsiga ei leita üles nii suurt osa haigetest kui soovitakse.
Glükohemoglobiini analüüsi tundlikkus võib olla veidi parem kui paastuglükoosi analüüs. Glükoositaluvuse proovi käsitleti vaid ühes süstemaatilises ülevaates (27), kus selle meetodi tundlikkus oli kolme seast väikseim. Spetsiifilisuse erinevus glükohemoglobiini ja paastuglükoosi analüüsi vahel ei ole väga selge, kuid võib kalduda paastuglükoosi analüüsi kasuks.
Vaadeldud analüüside negatiivne ennustusväärtus on väga hea (97,2–99,0%), kuid positiivne ennustusväärtus madal (5,4–22,9%). Uuringute tõlgendamist raskendab see, et teadustöödes on proovitulemuste tõlgendamisel kasutatud palju erinevaid diagnostilisi läviväärtuseid.
Töörühm võttis soovituse sõnastamisel arvesse nii paastuglükoosi analüüsiga kaasnevat korralduslikku keerukust tervishoiutöötajale ja ebamugavust inimesele inimene peab olema söömata) kui ka glükohemoglobiini testi suuremat kulukust. Kuna kahe meetodi diagnostilistes omadustes ei ole suuri erinevusi, täiendatakse ravijuhendi uuendamisel vajaduse korral soovitust uute teadusuuringute tulemuste põhjal.
Riskitegurite hindamine
Sümptomiteta täiskasvanutel lähtuge 2. tüüpi diabeedi varaseks avastamiseks järgmisest:
- Täiskasvanutel tuleks enne 45. eluaastat sõeluuringut kaaluda, kui esineb ülekaal võ i rasvumine (KMI ≥ 25 kg/m2 ) ning lisaks üks või mitu järgmist
riskitegurit (28):
• esimese astme sugulasel on diagnoositud 2. tüüpi diabeet;
• suure riskiga rass või etniline taust;
• anamneesis SVH;
• hüpertensioon (vererõhk ≥ 140/90 mmHg või tarvitab vererõhuravimit);
• HDL-Chol < 0,90 mmol/L või triglütseriidid > 2,82 mmol/L;
• polütsüstiliste munasarjade sündroom;
• vähene füüsiline aktiivsus;
• viited insuliiniresistentsusele. - Prediabeediga patsientidel (HbA1c vahemikus 6,0–6,4% või 42–47 mmol/mol ja/või esineb IFG või IGT) tuleks vere glükoosisisaldust mõõta vähemalt
üks kord aastas - Gestatsioonidiabeedi diagnoosiga naistel vähemalt iga kolme aasta tagant
- HIV-iga patsientidel
- Kõigil teistel täiskasvanutel tuleks sõelumist alustada alates 45. eluaastast. Kui vere glükoosisisaldus jääb normaalsesse vahemikku, tuleks sõeluuringut korrata vähemalt iga kolme aasta tagant.
Kui paastuglükoosi või glükohemoglobiini analüüsi tulemus viitab 2. tüüpi diabeedile, siis järgige diagnoosimises ja ravis juhendit „2. tüüpi diabeedi
diagnostika ja ravi“ (29).
Vaata lähemalt neljanda kliinilise küsimuse TõKo ja SoKo tabelit.
Eesnäärmevähk on Eesti meestel kõige sagedamini diagnoositud pahaloomuline kasvaja (30). Samas ei põhjusta eesnäärmevähk enim kasvajast tingitud surmasid (31).
Eesnäärmevähki diagnoositakse enim 60–75-aastastel (30). Sageduse tõttu saab teema palju kajastust ka meedias ning mehed pöörduvad sageli vastuvõtule
sooviga lasta teha PSA-analüüs ka siis, kui kaebuseid ei ole.
Kuigi rahvastikupõhise sõeluuringuga leitaks rohkem varases staadiumis kasvajaid, ei ole selge, kas nende varasem avastamine ja ravi muudaksid haiguse kulgu, sest eesnäärmevähk on tihti aeglase kuluga ning ei tekita sageli mehe eluajal kaebuseid ega põhjusta surma. PSA-analüüsi tegemine kaebuste ja riskiteguriteta inimesel nõuab lisauuringuid, põhjustab ülediagnoosimist ja suurendab invasiivse ravi vajadust meestel, kelle elulemus sellest ei paraneks ja kelle elukvaliteet võib seeläbi hoopis halveneda.
Eestis analüüsiti eesnäärmevähi rahvastikupõhise sõeluuringu kulutõhusust ja efektiivsust 2017. aastal (32) ning ei leitud, et see oleks kumbagi. Seetõttu
soovitati jätkata senise praktikaga. 2020. aastal koostati TTH raport (33), mille eesmärk oli ajakohastada hinnang eesnäärmevähi varase avastamise meetodite kasude kohta enne haigustunnuste tekkimist ehk sõeluuringu kontekstis ning analüüsida sõeluuringu rakendusvõimalusi Eestis. Raporti tulemusena soovitati Eestis teha eesnäärmevähi varase avastamise katseprojekt, millega selgitada välja usaldusväärsed sisendid, et hinnata sõeltestimise tegelikku kasu Eesti meestele.
Eesnäärmevähi varase avastamise katseprojekti eesmärk on hinnata eesnäärmevähi sõeluuringu teostatavust: sihtrühma meeste valmisolekut sõeluuringus osaleda, sõeluuringu logistikaplaani, riskihindamise mudeli võimekust tunda ära suure riskiga isikud, MRT leiu hindamise protokolli ning sõeluuringu ja jätku-uuringute tegelikku kulu. Mitte üheski läbi vaadatud ravijuhendis (34, 35, 36, 37, 38) ei soovitata rahvastikupõhist eesnäärmevähi sõelumist PSA-analüüsi kasutades.
Ravijuhendites tuuakse esile, et enne analüüsi tegemist peab andma patsiendile põhjaliku ülevaate analüüsiga kaasuvatest kasudest ja kahjudest (ebavajalikud
analüüsid, uuringud, ravi ja nende tüsistused). Ravijuhendites antud soovitustes jäetakse palju arsti ja patsiendi otsustada ning öeldakse, et otsus on indiviidipõhine, sõltub riskist ja patsiendi eelistustest ning peab olema teadlik.
9. 40–54-aastasel mehel hinnake enne PSA-analüüsi tegemist järgmiste eesnäärmevähi riskitegurite esinemist:
• eesnäärmevähi esinemine esimese astme sugulasel,
• rinnavähi esinemine esimese astme sugulasel,
• Aafrika päritolu.Nõrk positiivne soovitus, madal tõendatuse aste
10. 40–54-aastasele mehele, kellel esineb vähemalt üks eesnäärmevähi riskitegur, võite soovitada PSA-analüüsi tegemist.
Teavitage meest uuringu tulemusega seotud kasust ja kahjust.Nõrk positiivne soovitus, madal tõendatuse aste
11. 55–65-aastasele mehele võite soovitada PSA-analüüsi tegemist. Teavitage meest uuringu tulemusega seotud kasust ja kahjust.
Nõrk positiivne soovitus, madal tõendatuse aste
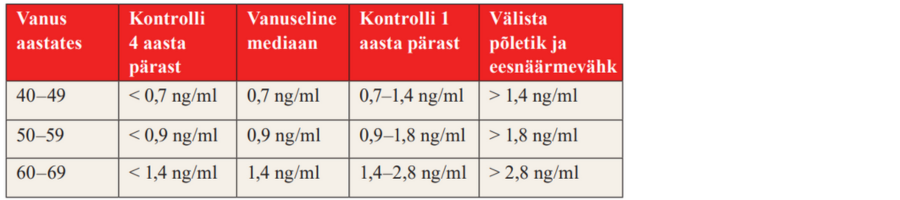
12. Lähtuge PSA-analüüside tõlgendamisel ja järgmise kontrolli vajaduse hindamisel ravijuhendi tabelist 3.
Praktiline soovitus
Tabel 3. PSA vanusespetsiifilised väärtused ja soovitused edasiseks jälgimiseks (39)
Tõendus PSA kontsentratsiooni määramise efektiivsuse kohta tervetel kaebusteta meestel pärines viie ravijuhendi (34, 35, 36, 37, 38) tõendusmaterjali seast leitud uusimal süstemaatilisel ülevaateuuringul (40). Lisaks vaadati eraldiseisvalt selle uuringu metaanalüüsi kaasatud kolme suurema juhuslikustatud kontrolluuringu – ERSPC (41), CAP (42) ja PLCO (43) – viimaseid tulemusi. Sirveotsinguga leiti veel üks metaanalüüs, mis käsitleb eesnäärmevähki suremust (44).
Suremus
Ilici jt (40) metaanalüüsis ei leitud, et PSA-põhine sõelumine oleks vähendanud üldsuremust. Üldsuremuse vähenemist ei täheldatud ka juhuslikustatud
kontrolluuringutes (41, 42). Ilici jt metaanalüüsis (40) ei leitud, et organiseeritud sõelumine vähendaks eesnäärmevähki suremust, kuid Pasheni jt metaanalüüsis (44) leiti statistiliselt oluline vähenemine.
ERSPC uuringus (41) leiti kogu sihtrühma (50–74-aastased mehed) ja põhirühma (55–69-aastased mehed) tulemuste analüüsis eesnäärmevähist tingitud suremuse statistiliselt oluline vähenemine. Viieaastaste vanusevahemike analüüsis ei olnud leid järjepidev – eesnäärmevähist tingitud suremus vähenes oluliselt 55–59-aastaste ja 64–69-aastaste meeste seas, kuid teistes vanuserühmades mitte.
Kahes teises juhuslikustatud kontrolluuringus, CAP-is (42) ja PLCO-s (43), ei leitud eesnäärmevähist tingitud suremuse vähenemist. CAP-i sihtrühmas olid 50–69-aastased mehed, kellel määrati PSA sisaldus ühe korra. PLCO-sse kaasati 55–74-aastased mehed, kellel määrati PSA sisaldus kord aastas kuue aasta jooksul.
Riskitegurid
Vanus
Tõendus vanuse kui eesnäärmevähi riskiteguri kohta pärines kahest metaanalüüsist (40, 45) ja eelmainitud uuringutest ERSPC ja CAP. Metaanalüüsides ei leitud, et võrreldes tavapraktikaga mõjutaks sõeluuringuga 45-, 50- või 55-aastaselt alustamine eesnäärmevähist tingitud suremust. Uuringu ERSPC (41) tulemused viieaastaste vanusevahemike kohta ei olnud järjepidevad – eesnäärmevähist tingitud suremus vähenes oluliselt 55–59-aastaste ja 64–69-aastaste meeste seas, kuid teistes vanuserühmades mitte.
Samas leiti oluline eesnäärmevähist tingitud suremuse vähenemine üldrühmas (50–74-aastased mehed) ja põhirühmas (55–69-aastased mehed). Viieaastaste vanuserühma vahemike analüüs tehti ka uuringus CAP (42), kuid selles uuringus ei leitud mitte üheski vanuserühmas, et eesnäärmevähist tingitud suremus oleks statistiliselt oluliselt vähenenud.
Töörühm võttis vanuse kui riskiteguri määratlemisel arvesse, et selle oli oma ravijuhendis riskitegurina esile toonud Euroopa Uroloogide Ühendus (38), kuid
tõendusena lisatud uuringu kvaliteet oli väga madal. Seetõttu otsustas töörühm pärast suurte juhuslikustatud kontrolluuringute tulemuste analüüsi lähtuda
kvaliteetseima ja ülesehituselt sobivaima uuringu ERSPC tulemustest. Selle uuringu 16-aastase jälgimisperioodi tulemuste analüüsis leiti, et eesnäärmevähist
tingitud suremus vähenes oluliselt 55–59-aastaste ja 65–69-aastaste meeste vanuserühmas. Seepärast otsustati soovitada PSA sisalduse vereanalüüsist
määramist kõigile üle 55-aastastele meestele, kellel seda pole varem tehtud või kelle viimast analüüsi peaks tabelis 3 toodud soovituste põhjal kordama.
Kasvajate pereanamnees
Tõendus selle kohta, et eesnäärmevähi pereanamneesis esinemine on riskitegur, pärines viiest uuringust (46, 47, 48, 49, 50). Neljas uuringus leiti, et eesnäärmevähi esinemine nii esimese kui ka teise astme sugulasel suurendab eesnäärmevähi tekke riski (46, 47, 48, 50). Ühes süstemaatilises ülevaateuuringus (49) ja ühes kohortuuringus (46) ei leitud, et peres eesnäärmevähi esinemine oleks mõjutanud eesnäärmevähist tingitud suremust. Kahes teises kohortuuringus (47, 48) leiti, et eesnäärmevähi peres esinemise korral oli suurenenud risk surmaga lõppeva eesnäärmevähi esinemiseks. Tõendus selle kohta, et rinnavähi pereanamneesis esinemine on riskitegur, pärines ühest metaanalüüsist (51). Leiti, et rinnavähi esinemine esimese astme sugulasel suurendas eesnäärmevähi avaldumise ja surmaga lõppeva eesnäärmevähi esinemise riski.
Aafrika päritolu
Tõendus Aafrika päritolu kui riskiteguri kohta pärines ühest juhuslikustatud kontrolluuringust (52), milles leiti, et Aafrika päritolu meeste seas on suuremad
eesnäärmevähist tingitud suremus ja ka selle avaldumus.
Soovimatu mõju
Tõendus soovimatu mõju kohta pärines kahest süstemaatilisest ülevaateuuringust (40, 44) ja kahest juhuslikustatud kontrolluuringust (53, 54). Uuringutes (44, 53, 54) leiti, et vähemalt ühe valepositiivse tulemuse võib saada 4–19% meestest ning nende seas, kellele tehakse kolm või enam analüüsi, võib valepositiivseid tulemusi olla 11–26%-l (44). Pasheni jt metaanalüüsis (44) leiti, et PSA-põhise sõelumisega on risk ülediagnoosimiseks 7–60 juhul 1000 kutsutud mehe kohta.
Eesnäärmevähi diagnoosi võib põhjendamatult saada 35–60 meest 1000 mehe kohta. Biopsiast tulenevaid tüsistusi esines valepositiivse tulemuse saanud meeste seas 22,6 mehel 1000-st. Pasheni jt metaanalüüsi järgi tehtaks valepositiivse tulemuse tõttu 223–261 mehele 1000 skriiningul osalenud mehe kohta vähemalt üks biopsia ning neist 5–6 mehel tekiks biopsiaga seotud tüsistus.
Järeldati, et sõelumisega seotud kahju – ülediagnoosimine ja suur valepositiivsete tulemuste hulk – on suurem kui saadav kasu. Lisaks tekib sõelumisel kahju väga varakult ja selle mõju võib olla eluaegne. Ilic jt (40) leidsid, et pärast eesnäärmevähi ravi tekkis 1000 sõelutud mehe seas uriinipidamatust kolmel mehel rohkem ja erektiilset düsfunktsiooni 25 mehel rohkem kui sõelumata meeste seas.
Väärtushinnangud
Tõendus väärtushinnangute kohta pärines ühest süstemaatilisest ülevaateuuringust (55), milles järeldati, et sõeluuringus osalemise otsus sõltub suuresti mehe eelistustest ja peab olema langetatud koos arstiga. Ei leitud ühtegi uuringut, mis võrdleks seda, kas väärtushinnangud ja eelistused erinevad riskiteguritega (positiivne pereanamnees, Aafrika päritolu, madal sotsiaalmajanduslik staatus) ja riskiteguriteta meeste seas.
Töörühm võttis soovituste sõnastamisel arvesse, et siinne ravijuhend käsitleb võimalusepõhiseid tervisekontrolle, tõendusmaterjalides käsitletakse aga PSA-põhist süstemaatilist sõelumist. Lisaks arvestas töörühm, et lähiaastail on Eestis plaanis teha eesnäärmevähi sõeluuringu katseprojekt, mille tulemuste põhjal
muudetakse vajaduse korral ravijuhendi soovitusi. PSA puhul kasutatakse haigusliku muutuse ja normi eristamiseks kokkuleppelist piirväärtust, kuid
ravijuhendite soovitustes pole konsensust, millise läviväärtuse korral saaks panna kindla diagnoosi või öelda, millal suunata patsient edasi uroloogile.
Seepärast soovitas töörühm lähtuda Eesti Arstis avaldatud ravijuhendi „Meeste kusemishäirete käsitlus- ja ravijuhend perearstidele“ (39) soovitustest, mis on
esitatud selle ravijuhendi tabelis 3.
Lisamaterjal PSA-põhist sõeluuringut puudutavate küsimuste kohta on esitatud lisas 3. Materjal on abiks arsti ja patsiendi vahelisel vestlusel.
Vaata lähemalt üheksanda kliinilise küsimuse TõKo ja SoKo tabelit.
Glaukoomi varane avastamine on äärmiselt oluline, et vältida nägemist mõjutavate tõsiste tüsistuste teket. On leitud, et USA-s on glaukoom pöördumatu pimeduse tekkepõhjusena teisel kohal ja mõjutab seega umbes 2,7 miljonit inimest (56).
Primaarset avatud nurgaga glaukoomi on hea tuvastada just sõeluuringuga, sest patsiendid on haiguse hilise faasini enamasti asümptomaatilised (57).
13. 40–65-aastaselt inimeselt küsige, kas kellelgi tema esimese astme sugulastest on esinenud glaukoom.
Nõrk positiivne soovitus, väga madal tõendatuse aste
14. 40–65-aastane inimene, kelle esimese astme sugulasel on diagnoositud glaukoom, suunake oftalmoloogi vastuvõtule.
Praktiline soovitus
Tõendusmaterjal glaukoomi varase avastamise kohta pärineb peamiselt USPSTF-i 2022. aasta ravijuhendi (56) tarbeks koostatud süstemaatilisest ülevaatest (58).
Ülevaatesse kaasati 40-aastased ja vanemad inimesed, kes pöördusid esmatasandi tervishoiutöötaja poole ilma glaukoomi tunnuste ja sümptomiteta. Ülevaatesse kaasati üks juhuslikustatud kontrolluuring (59), mis tehti Austraalia põdurate vanemaealiste inimeste hulgas. Uuringus võrreldi optometristi tehtud nägemise sõeluuringut (sh tonomeetria ja perimeetria) selle tegemata jätmisega. Uuringust selgus, et aastase jälgimisperioodi möödumisel ei olnud kahe rühma vahel olulist erinevust nägemisparameetrites ega ka nägemisega seotud elukvaliteedis.
Lisaks leiti, et glaukoomi sõeluuring oli seotud suurenenud kukkumisriskiga. Kukkumisriski suurenemise põhjus jäi ebaselgeks, kuid tulemuste tõlgendamisel
on oluline teada, et 46% uuritavatest olid uuringule eelneva aasta jooksul juba kukkunud. Seega võib järeldada, et glaukoomi sõeluuringu kasu ja kahju tasakaalu hindamiseks on tõendusmaterjal praegu ebapiisav.
Hollandsi jt süstemaatilisse ülevaatesse (60) kaasati rahvastikupõhised uuringud. Tulemustest selgus, et kui esimese astme sugulasel on esinenud glaukoom, on see primaarse avatud nurgaga glaukoomi puhul üks olulisemaid riskitegureid. Chou jt süstemaatilises ülevaates (58) hinnati ka tonomeetria ja perimeetria täpsust glaukoomi diagnoosimisel. Leiti, et tonomeetria on glaukoomi diagnoosimisel kõrge spetsiifilisusega, kuid vähese tundlikkusega. Perimeetria täpsuse hindamisel selgus, et Humphrey nägemisvälja mõõtmise vahend (ingl Humphery visual field analyzer) on glaukoomi diagnoosimisel aktsepteeritava täpsusega: meetodi tundlikkus oli 0,87 ja spetsiifilisus 0,82.
Töörühm võttis soovituse sõnastamisel arvesse, et tonomeetria üksi ei ole glaukoomi diagnoosimiseks piisav meetod, kuna glaukoom võib esineda ka siis, kui silma siserõhk on normipärane. Samuti leiti, et perimeetria ei pruugi olla esmatasandil kättesaadav. Eesti Oftalmoloogide Seltsi hinnangul võiksid perearstid küsida patsiendilt, kas tema lähisugulasel esineb glaukoomi. Suure glaukoomiriski tuvastamisel tuleks patsient suunata plaaniliselt oftalmoloogi ambulatoorsele vastuvõtule.
Vaata lähemalt kuuenda kliinilise küsimuse TõKo ja SoKo tabelit.
Osteoporoosi puhul on peamine probleem haprusmurru riski suurenemine, mis tingib patsientide sagedasema haigestumise ja oodatava eluea languse.
Osteoporoosi on oluline varakult diagnoosida, et alustada ravi õigeaegselt, vähendada seekaudu luumurru riski ja tekkivaid ravikulusid ning parandada
kliinilist tulemust (61).
15. 40–65-aastasel naisel võite osteoporoosi riski hindamiseks kasutada luumurruriski kalkulaatorit FRAX.
Nõrk positiivne soovitus, väga madal tõendatuse aste
16. 40–65-aastane naine suunake luudensitomeetria uuringule, kui luumurruriski kalkulaatori FRAX järgi on kümne aasta reieluukaela murru risk ≥ 2% ja üldine luumurru risk ≥ 6%.
Praktiline soovitus
17. 40–65-aastast naist nõustage osteoporoosi riskitegurite suhtes.
Praktiline soovitus
Olemasolev tõendusmaterjal osteoporoosi suhtes sõelumise soovitud mõju kohta pärineb peamiselt USPSTF-i 2018. aasta ravijuhendi (62) uuendamise tarbeks koostatud süstemaatilisest ülevaatest (63). Ülevaatesse kaasati osteoporoosi sõelumise efektiivsuse hindamiseks juhuslikustatud kontrolluuring SCOOP („The Screening for Osteoporosis in Older Women for the Prevention of Fracture“) (64), milles osales 12 483 70–85-aastast naist. Uuringus võrreldi luumurruriski kalkulaatori FRAX abil osteoporoosi suhtes sõelumist mittesõelumisega ning uuritavate puhul hinnati kalkulaatoriga reieluukaela murru kümne aasta riski.
Uuringu tulemuste põhjal saab järeldada, et FRAX-i abil osteoporoosi suhtes sõelutud naiste seas esines viie aasta möödumisel statistiliselt olulisel määral
vähem reieluukaela murde kui mittesõelutud uuritavate seas. Osteoporoosi suhtes sõelutud ja mittesõelutud naiste seas ei esinenud olulist erinevust soovimatus mõjus (hinnati elukvaliteeti ja ärevuse esinemist).
FRAX-iga osteoporoosi riskiskoori arvutamiseks arvestatakse järgmisi riskitegureid: vanus, sugu, pikkus, kaal, varasem luumurd, vanemate reieluukaela murd, tubaka- ja nikotiinitoodete tarvitamine, alkoholitarvitamine, glükokortikosteroidravi, reumatoidartriit, sekundaarne osteoporoos ja luutihedus
(saab arvutada ka ilma luutiheduse näitajata). Vaata täpsemalt veebilehelt FRAX “Murruriski kalkulaator”.
FRAX-i tulemuste tõlgendamisest ei ole Eestis uuringuid avalikustatud, kuid kalkulaatori koostajad on tõlgenduse Eesti elanikkonna 50–65-aastaste isikute
puhul välja selgitanud¹. On leitud, et osteoporoosi võimalikult varaseks avastamiseks võiks patsiendi suunata luudensitomeetriasse juhul, kui FRAX-i
alusel on reieluukaela murru risk ≥ 2% ja murru üldine risk ≥ 6%. need väärtused on osteoporoosi ravi alustamise lävendid. Kui densitomeetria on varem tehtud, siis on lävendid vastavalt ≥ 3% ja ≥ 10%.
¹ Käesolev FRAX küsimustiku tõlgendus tugineb publitseerimata andmetel, mis põhinevad vestlusel Eesti uuringu läbi viinud reumatoloog dr. Mart Kulliga.
Osteoporoosi riskitegurid saab tõendusmaterjali alusel jagada kaheks: mittemuudetavateks ja muudetavateks. Osteoporoosi puhul on tähtsad mittemuudetavad riskitegurid varasem haprusmurd, varane menopaus, vanus, naissugu, valge rass, vanematel esinenud reieluukaela murd või osteoporoos.
Tõendusmaterjal mittemuudetavate riskitegurite kohta pärines kokku seitsmest allikast, mille hulgas on jälgimisuuringud ja nendel põhinevad süstemaatilised ülevaated (65, 66, 67, 68, 69, 70, 71). Muudetavate riskiteguritena saab aga esile tuua tubaka- ja nikotiinitoodete tarvitamise, alkoholitarvitamise, vähese füüsilise aktiivsuse, madala kehamassiindeksi ning pikaajalise süsteemse glükokortikosteroidravi. Tõendusmaterjal muudetavate riskitegurite kohta pärineb samuti mitmest jälgimisuuringust ja süstemaatilistest ülevaadetest (66, 72, 73, 74, 75).
Töörühm võttis soovituse sõnastamisel arvesse, et kõigis Eesti piirkondades ei pruugi olla luudensitomeetria võrdselt kättesaadav, kuid töörühma hinnangul
ei vaja probleem kiiret käsitlust. Kuigi teaduskirjanduses on leitud, et suurem osteoporoosi risk on naistel, arvestas töörühm sellega, et ainult naistele suunatud soovitus võib vähendada tervisevõimaluste võrdsust.
Kui luudensitomeetria uuringuga kinnitatakse osteoporoosi diagnoos, võiks seni, kuni puudub Eesti osteoporoosi ravijuhend, lähtuda ravis Eesti Reumatoloogia Seltsi soovitusel Euroopa 2019. aasta ravijuhendist (76). Eesti ravijuhendiga alustatakse tööd sügisel 2023.
Vaata lähemalt viienda kliinilise küsimuse TõKo ja SoKo tabelit.
Sellistes vähese päikesepaistelise ajaga maades nagu Eesti räägitakse D-vitamiini lisamanustamise vajadusest sügis-talvisel perioodil. Lisaks tunnevad inimesed huvi D-vitamiini sisalduse määramise vastu vereanalüüsist. Selle tõenduspõhisusest räägitakse aga vähe ja puuduvad täpsed soovitused lisamanustamise perioodi, sageduse ja annuse kohta.
Eesti 2015. aasta toitumis- ja liikumissoovitustes (77), kirjutatakse, et 6-kuused kuni 60-aastased inimesed vajavad päevas 10 mcg (400 RÜ ehk rahvusvahelist ühikut) ning üle 60-aastased 20 mcg (800 RÜ) D-vitamiini. Lisatarbimine rikastatud toitudest või D3-vitamiini rasvlahustuva preparaadina kuni 10 mcg (400 RÜ) päevas võib olla vajalik juhul, kui tavatoit ja õuesviibimine ei taga piisavat vitamiinikogust. Erilist tähelepanu tuleb siinjuures pöörata tubase eluviisiga isikutele, et tagada nende D-vitamiini tarve.
18. Kui on kahtlus, et inimene ei saa toidust piisavalt D-vitamiini, nõustage teda tervisliku toitumise teemal, lähtudes Eesti toitumis- ja liikumissoovitustest.
Praktiline soovitus
19. Tubase eluviisiga inimest nõustage füüsilise aktiivsuse ja õues viibimise teemal.
Praktiline soovitus
20. 40–65-aastasele inimesele võite soovitada D-vitamiini lisamanustamist 10–25 µg/päevas (400–1000 RÜ), kui tekib kahtlus, et inimene ei saa piisavalt D-vitamiini.
Nõrk positiivne soovitus, madal tõendatuse aste
21. D-hüpovitaminoosi kahtluseta 40–65-aastasel inimesel pigem ärge määrake D-vitamiini sisaldust veres.
Praktiline soovitus
Tõendust D-vitamiini lisamanustamise kohta vereanalüüsist määratud D-vitamiini sisalduse alusel ei leitud. Tõendus D-vitamiini lisamanustamise mõju kohta tulemusnäitajatele (luumurrud, üldsuremus) pärines seitsmest süstemaatilisest ülevaateuuringust (78, 79, 80, 81, 82, 83, 84) ning mõju luumurdudele analüüsiti viies uuringus (78, 80, 82, 83, 84).
Mitte üheski neist ei leitud, et D-vitamiini lisamanustamine oleks vähendanud igasuguste luumurdude või puusapiirkonna luumurdude (ingl hip fracture) esinemist või nende riski. D-vitamiini lisamanustamise mõju üldsuremusele analüüsiti neljas uuringus (79, 81, 83, 84), millest kahes (83, 84) ei leitud mõju ja kahes teises (79, 81) leiti mõju mõne alarühma analüüsis, mis aga ei kuulunud selle juhendi sihtrühma.
Kõrvaltoimeid esines uuringutes sekkumis- ja kontrollrühmas sarnasel määral (84). Kõige sagedamini tekkisid neerukivid, kuid selle kohta käiv tõendus ei olnud hea kvaliteediga ja leiud ei ühtinud (81, 83, 84).
D-vitamiini annuste kohta pärineb tõendus neljast süstemaatilisest ülevaatest.
2017. aastal avaldatud süstemaatilises ülevaates hinnati seost D-vitamiini annuse ja seerumi 25(OH)D sisalduse vahel. Leiti, et seerumi 25(OH)D väärtuste > 25, > 30 ja > 50 nmol/L tagamiseks on vajalikud D-vitamiini annused vastavalt 10, 13 ja 26 µg ööpäevas (85).
Uuringutes, kus võrreldi D-vitamiini eri annuste (< 800 RÜ ööpäevas või > 800 RÜ ööpäevas) mõju suremusele (võrdlusrühmas olnud said kas platseebot või ei sekkutud), leiti, et väiksemas annuses D-vitamiini saanud uuritavatel vähenes suremus statistiliselt olulisel määral, suurema annuse puhul erinevust polnud. Alarühmasid omavahel võrreldes aga rühmade vahel erinevust ei leitud (79, 81). Ühes uuringus (80) hinnati D-vitamiini mõju luumurdude tekkele.
Lisaanalüüsina võrreldi annuseid neljas alarühmas, kus pooled uuritavad said platseebot ja teised vastavalt D-vitamiini ≥ 800 RÜ päevas, < 800 RÜ päevas,
kõrgdoosis üks kord aastas või kõrgdoosis muu sagedusega. Ühegi rühma sees tulemusnäitajas erinevusi ei leitud. Samuti ei olnud erinevusi alarühma analüüside vahel.
Töörühm võttis soovituste sõnastamisel arvesse, et mitte üheski AGREE II-ga hinnatud ravijuhendis (34, 83, 84, 86) ei soovitatud D-vitamiini lisamanustamist kogu elanikkonnale. Tervishoiusüsteemi vaatepunktist ja ravijuhendite soovitustest lähtuvalt peaks D-vitamiini sisaldust vereanalüüsist määrama vaid inimestel, kellel esinevad selle puudulikkusele omased kaebused või kui inimese eluviisi põhjal on kahtlus puudulikkuse esinemisele.
Lisaks võeti arvesse Eesti toitumisja liikumissoovitusi, milles soovitatakse D-vitamiini soovitada neile, kel esineb suurenenud risk D-vitamiini puudulikkuse tekkeks: tubase eluviisiga inimesed, eridieete pidavad inimesed (nt taimetoitlased, täistaimetoitlased), tumeda nahaga inimesed, aasta ringi katvaid riideid kandvad inimesed, rasvunud inimesed. Eridieetide puhul tasub esmalt täpsustada, mida inimene on oma söögilaualt välja jätnud ja kui palju ta õues viibib.
Töörühm võttis soovituste sõnastamisel arvesse, et D-vitamiini lisamanustamise soovitusest tähtsam on nõustada inimesi õuesviibimise ja mitmekülgse toitumise olulisuse teemal.
Vaata lähemalt seitsmenda ja kaheksanda kliinilise küsimuse TõKo ja SoKo tabelit.
Depressiooni läbilõikeline levimus Eestis on hinnanguliselt 5,9% ja ärevushäirete levimus 3,2%, mis on ühed Euroopa suurimad (87). Seejuures on depressiooni levimus vanuses 40–60 aastat reeglina elukaare suurim: Tervise Arengu Instituudi Eesti terviseuuringu andmetel oli 2019. aastal depressiooni levimus vanuserühmades 55–64 ja 45–54 vastavalt 10,9% ja 10,2% (88).
Depressiooni ja ärevushäiretega patsientide varaseks tuvastamiseks on levinud soovitus kasutada sõelumisvahendina enesekohaseid küsimustikke, sh esmatasandil (89). Eestis on välja töötatud emotsionaalse enesetunde küsimustik, mille teist täiendatud versiooni EEK-2 kasutatakse sageli nii kliinilises praktikas kui ka teadustöös (90). Ingliskeelses teaduskirjanduses kajastatakse veel paljusid sõelteste, mille omadused on suhteliselt sarnased.
Et tagada tõhus depressiooni ja ärevushäirete varane tuvastamine ja samas võimalikult efektiivne personali- ja ajakasutus, sobib hästi heade omaduste ja võimalikult väikse ajakuluga sõeltest.
22. 40–65-aastasel inimesel kasutage depressiooni esmaseks hindamiseks küsimustikke PHQ-2 või EEK-2.
Tugev positiivne soovitus, mõõdukas tõendatuse aste
23. 40–65-aastasel inimesel võite kasutada ärevushäire esmaseks hindamiseks küsimustikke GAD-2 või EEK-2.
Nõrk positiivne soovitus, madal tõendatuse aste
Tõenduse analüüsi kaasati 16 metaanalüüsi või süstemaatilist ülevaadet, neist 13 depressiooni suhtes (90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101)
ning kolm ärevushäire suhtes sõelumise kohta (102, 103, 104). Vaatamata varieeruvale tõendatuse astmele on ka lühikesed sõeltestid hea tundlikkuse
ja üpris hea spetsiifilisusega.
Eestikeelse EEK-2 tundlikkus jääb depressiooni puhul vahemikku 0,79–0,86 ja spetsiifilisus vahemikku 0,77–0,84 (vastavalt skoori äralõikepunktidega 10, 11 ja 12) (90). Välismaistest küsimustikest oli ühe küsimusega sõeltestide tundlikkus üsna madal, kuid kahe küsimusega küsimustike tundlikkus oli metaanalüüsides juba vahemikus 0,72–0,97 ja spetsiifilisus 0,67–0,87, eristumata oluliselt pikemate küsimustike näitajatest (91, 92, 93, 94, 95, 96).
Arvestades patsiendi anamneesi, ajakriitilisust ning isiklikke eelistusi, saab arst langetada otsuse, kas hindamiseks kasutatakse lühiküsimustikke PHQ2 või GAD-2 või põhjalikumat küsimustikku EEK-2 (vt lisa 4). Soovitatud küsimustikud on sõeluuringuks, mitte diagnostilised vahendid ja lävendi ületanud
patsiendid vajavad lisauurimist. Samuti rõhutatakse paljudes teadusuuringutes ja ravijuhendites, et sõeluuringul puudub mõte, kui sõelumisele ei järgne sekkumist (ravi ja jälgimist).
Töörühm võttis soovituste sõnastamise juures arvesse ka nii välismaiste küsimustike tõlkimise ja valideerimisega kaasnevaid kulusid kui ka asjaolu, et uue
lühema instrumendi kasutamine võib tänu väiksemale ajakulule olla patsiendile ja spetsialistile vastuvõetavam ning tagada paremini vahendi pideva kasutamise.
Läbiv hindamisvahendi rakendamine võiks ühtlustada diagnoosini jõudvate patsientide määra, nt piirkondade või sotsiaalsete gruppide vahel. PHQ-2 ja GAD-2 tehakse ravijuhend lisana kättesaadavaks pärast nende küsimustike Eestis valideerimist. Ravijuhendi koostamise ajal alustas Tervisekassa valideerimise protsessiga.
Kui sõeluuringu tulemus viitab depressiooni või ärevushäire olemasolule, siis kasutage diagnoosimiseks ja raviks ravijuhendeid „Depressiooni ravijuhend
perearstidele“ (105) ja „Generaliseerunud ärevushäire ja paanikahäire (agorafoobiaga või ilma) käsitlus perearstiabis“ (106).
Vaata lähemalt esimese kliinilise küsimuse TõKo ja SoKo tabelit.
Kehaline aktiivsus
24. 40–65-aastaselt inimeselt küsige.
• mitmel päeval nädalas on ta kehaliselt aktiivne,
• millise intensiivsusega on tema kehaline aktiivsus,
• mitu minutit korraga on ta kehaliselt aktiivne.
Vajaduse korral nõustage teda (vt lisa 5).Praktiline soovitus
Nõustamisel saate kasutada Eesti toitumis- ja liikumissoovitusi (77) või ravijuhendi lisa 5.
Toitumine
25. 40–65-aastaselt inimeselt küsige toitumise kohta ja uurige, milline osakaal on tema menüüs järgmistel toiduainetel:
• küllastumata rasvhappeid sisaldavad toidud (rasvane kala, pähklid ja seemned, avokaado, oliivid, taimeõli);
• kiudainerikkad taimsed toidud (köögiviljad, täisteratooted, kaunviljad, puuviljad ja marjad);
• punane ja töödeldud liha (võrreldes kala, linnuliha ja munaga);
• lisatud suhkur (nt suhkruga karastusjoogid), ohtralt suhkruid ja rasvu sisaldavad toidud (nt maitsestatud jogurtid);
• sool.
Vajaduse korral nõustage teda (vt lisa 5).Praktiline soovitus
Hinnake inimese toiduvalikuid seoses haigusriskidega ja andke toitumissoovitusi, et riske vähendada. Uurige, mida oleks inimene valmis oma toitumises muutma. Nõustamisel saate kasutada Eesti toitumis- ja liikumissoovitusi (77) või ravijuhendi lisa 5.
Tervislike eluviiside soovitused
Vähene kehaline aktiivsus, ülekaal, tasakaalustamata toitumine, alkoholi, tubakatoodete ja narkootikumide tarvitamine on paljude haiguste riskitegurid.
Eluviiside peatükk on tervishoiutöötajale abiks patsiendilt tema eluviiside kohta küsimisel. Eluviisi teemal nõustamiseks on koostatud „Tervislike eluviiside soovitused“ (lisa 5), kuhu on koondatud olulisemate juhendite soovitused ja viited asjakohastele veebilehtedele.
Kehaline aktiivsus
24. 40–65-aastaselt inimeselt küsige.
• mitmel päeval nädalas on ta kehaliselt aktiivne,
• millise intensiivsusega on tema kehaline aktiivsus,
• mitu minutit korraga on ta kehaliselt aktiivne.
Vajaduse korral nõustage teda (vt lisa 5).Praktiline soovitus
Nõustamisel saate kasutada Eesti toitumis- ja liikumissoovitusi (77) või ravijuhendi lisa 5.
Toitumine
25. 40–65-aastaselt inimeselt küsige toitumise kohta ja uurige, milline osakaal on tema menüüs järgmistel toiduainetel:
• küllastumata rasvhappeid sisaldavad toidud (rasvane kala, pähklid ja seemned, avokaado, oliivid, taimeõli);
• kiudainerikkad taimsed toidud (köögiviljad, täisteratooted, kaunviljad, puuviljad ja marjad);
• punane ja töödeldud liha (võrreldes kala, linnuliha ja munaga);
• lisatud suhkur (nt suhkruga karastusjoogid), ohtralt suhkruid ja rasvu sisaldavad toidud (nt maitsestatud jogurtid);
• sool.
Vajaduse korral nõustage teda (vt lisa 5).Praktiline soovitus
Hinnake inimese toiduvalikuid seoses haigusriskidega ja andke toitumissoovitusi, et riske vähendada. Uurige, mida oleks inimene valmis oma toitumises muutma. Nõustamisel saate kasutada Eesti toitumis- ja liikumissoovitusi (77) või ravijuhendi lisa 5.
Tubaka- või nikotiinitoodete tarvitamine
26. 40–65-aastaselt inimeselt küsige tubaka- ja nikotiinitoodete tarvitamise kohta. Kui ta tarvitab mainitud tooteid, siis nõustage teda ravijuhendi „Tubaka- või nikotiinitoodetest loobumise nõustamine“ põhjal.
Praktiline soovitus
Alkoholitarvitamine
27. 40–65-aastase inimese alkoholitarvitamise hindamiseks kasutage AUDIT-testi. Alkoholi liigtarvitamise kahtluse korral (skoor ≥ 8 punkti) tehke lühisekkumine ja edasisel käsitlusel lähtuge ravijuhendist „Alkoholitarvitamise häirega patsiendi käsitlus“.
Praktiline soovitus
Narkootiliste ainete tarvitamine
28. 40–65-aastaselt inimeselt küsige narkootiliste ainete tarvitamise kohta.
Praktiline soovitus
Kui inimene tarvitab narkootilisi aineid, siis võite sõelumiseks ja üldhinnangu andmiseks soovitada DUDIT-it (ingl drug use disorders identification test). Test on kättesaadav kodulehel https://www.narko.ee/testid/dudit-test-narkootikumidetarvitajale/.
Opioidisõltuvusega inimestele on Eestis kättesaadavad järgmised ravivõimalused:
- ambulatoorne opioidisõltuvuse asendusravi (üle Eesti);
- statsionaarne lühiajaline võõrutusravi (Viljandi Haigla või Wismari Haigla);
- pikaajaline statsionaarne võõrutusravi (Viljandi Haigla);
- pikaajaline statsionaarne rehabilitatsioon (Viljandi Haigla Sillamäe ja Viljandi osakonnad).
Kahjude vähendamise keskuste info leiate veebilehelt https://www.narko.ee/siitsaad-abi/kahjude-vahendamise-keskused-ohutumaks-tarvitamiseks/.
29. 40–65-aastase inimese immuniseerimise vajaduse hindamisel lähtuge Terviseameti täiskasvanute vaktsineerimise juhistest.
Praktiline soovitus
Täiskasvanute vaktsineerimise kohta on info olemas veebilehel https://www.vaktsineeri.ee/et/taiskasvanutele-vaktsineermine.
Vanuseline vaktsineerimiskava on veebilehel https://www.vaktsineeri.ee/et/taiskasvanutele/ajakava.
Kogu vaktsineerimise kohta käiva info leiate veebilehelt www.vaktsineeri.ee.
30. 40–65-aastasele inimesele soovitage sõeluuringutes osalemist riikliku sõeluuringute korralduse alusel.
Praktiline soovitus
Eestis kutsutakse rinnavähi sõeluuringule 50–68-aastaseid naisi iga kahe aasta tagant, emakakaelavähi sõeluuringule 30–65-aastaseid naisi iga viie aasta tagant ning jämesoolevähi sõeluuringule 60–68-aastaseid mehi ja naisi iga kahe aasta tagant. Sõeluuringutel saavad osaleda ka ravikindlustuseta inimesed.
Asjakohane info sõeluuringute kohta on kättesaadav Tervisekassa veebilehel www.soeluuring.ee.
31. Soovitage kord aastas HIV-testimist 40–65-aastasele inimesele, kes kuulub riskirühma*, või isikule, kel on diagnoositud HIViga seotud indikaatorseisund(id), aga kellel ei ole positiivset HIV-testi tulemust ega diagnoositud HIV-infektsiooni.
Praktiline soovitus
* Riskirühma kuuluvad narkootikume süstivad või süstinud inimesed, prostitutsiooni kaasatud inimesed, meestega seksivad mehed, nimetatud inimeste sekspartnerid, inimesed, kellel on olnud vahekord HIV-positiivse inimesega, inimesed, kellel on olnud mitu juhupartnerit ja kaitsmata vahekord.
HIV-testimise kohta saab täpsemalt lugeda „HIV-testimise ravijuhendist“ (107).
Lisas 6 on esitatud HIV-testimise algoritm.
LISAD
Ravijuhend ei asenda tervishoiutöötaja individuaalset vastutust teha õigeid (ravi)otsuseid konkreetsest inimesest lähtudes.
Ravijuhend “40–65-aastase täiskasvanu tervise jälgimise ja haiguste ennetamise juhend”
Kinnitatud: 03.07.2023
Avaldatud: 04.10.2023
Erialad/teemad: Terviseseisundit mõjustavad tegurid ja kontaktid terviseteenistusega [Z00-Z99]
Juhendi kood: RJ-Z/64.1-2023
Ravijuhend “40–65-aastase täiskasvanu tervise jälgimise ja haiguste ennetamise juhend” on leitav veebilehel: Ravijuhend.ee SIIN.
Ravijuhendite koostamist koordineerib Tartu Ülikool ja rahastab Tervisekassa.
Ravijuhend on valminud Tervisekassa rahastusel ja „Eesti ravijuhendite koostamise käsiraamatu“ (2020) järgi (www.ravijuhend.ee) /Eesti ravijuhendite koostamise käsiraamat 2020. Eesti Haigekassa 2021/.
- Ravijuhend on avaldatud Tervisekassa loal.
Töörühma liikmed
Sekretariaadi liikmed
| Määratlus | Hinnang |
|---|---|
| Töörühm on väga kindel, et tegelik mõju on hinnangulisele mõjule lähedal. | Kõrge |
| Töörühm on mõju hinnangus mõõdukalt kindel: tegelik mõju on tõenäoliselt lähedane hinnangulisele mõjule, kuid võib sellest ka märgatavalt erineda. |
Mõõdukas |
| Töörühm ei ole mõjuhinnangus eriti kindel: tegelik mõju võib märgatavalt erineda hinnangulisest mõjust. |
Madal |
| Töörühm ei ole mõjuhinnangus üldse kindel: on tõenäoline, et tegelik mõju erineb hinnangulisest mõjust märgatavalt |
Väga madal |
Tugeva soovituse andmisel on ravijuhendi koostajad kindlad, et soovituse järgimise oodatavad tulemused kaaluvad üles ebasoodsa mõju. Soovitus võib olla sekkumise poolt või vastu.
Nõrga soovituse andmisel arvavad töörühma liikmed, et selle täitmise oodatavad tulemused ületavad ebasoodsat mõju, kuid nad ei ole selles kindlad. Ebakindlust võib põhjustada
- kõrge või mõõduka astme tõendusmaterjali puudumine;
- vastuolulised hinnangud kasu ja kahju kohta;
- ebakindlus või erinevused selles, kuidas üksikisikud tervisetulemeid väärtustavad;
- vähene tervisekasu;
- selline tervisekasu, mis ei ole kulusid väärt (k.a soovituste rakendamise kulud).
Soovituse usaldusväärsuse huvides peab ravijuhendi töörühm kaaluma kõiki teadaolevaid tegureid ja põhjendama oma otsuste põhjuseid üksikasjalikult.
Kindel soovitus antakse vaid juhul, kui sekkumine või ravim vastab Eesti tervishoiusüsteemi suutlikkuse nõuetele.
Ravijuhend võib sisaldada suuniseid ehk praktilisi soovitusi, mis põhinevad ravijuhendi töörühma liikmete kliinilisel kogemusel ja eksperdiarvamusel ning võivad olla praktikas abiks parima ravitulemuse saavutamisel.
Südame-veresoonkonnahaiguste varane avastamine
1. 40–65-aastasel inimesel kasutage kardiovaskulaarse riski hindamiseks riskiskoori SCORE2.
Tugev positiivne soovitus, madal tõendatuse aste
Suure südame-veresoonkonnahaiguste riskiga inimeste statiinravi ja ravieesmärgid
2. Riskiskoori SCORE2 hinnangu alusel väga suure südameveresoonkonnahaiguste riskiga 40–65-aastasele inimesele määrake statiinravi.
Tugev positiivne soovitus, mõõdukas tõendatuse aste
3. Riskiskoori SCORE2 hinnangu alusel suure südameveresoonkonnahaiguste riskiga 40–65-aastasel inimesel hinnake enne statiinraviga alustamist eluviisimuutuste vajadust ning vajaduse korral nõustage teda.
Praktiline soovitus
4. Riskiskoori SCORE2 hinnangu alusel suure südameveresoonkonnahaiguste riskiga 40–65-aastasele inimestele kaaluge statiinravi määramist.
Nõrk positiivne soovitus, mõõdukas tõendatuse aste
5. Riskiskoori SCORE2 hinnangu alusel suure või väga suure südame-veresoonkonnahaiguste riskiga 40–65-aastasel inimesel eelistage suure intensiivsusega statiine.
Praktiline soovitus
6. Väga suure südame-veresoonkonnahaiguste riskiga 40–65-aastase inimese LDL-kolesterooli ravieesmärk on ˂ 1,4 mmol/L ja LDL-kolesterooli sisalduse vähenemine 50% või enam algsest LDL-kolesterooli väärtusest.
Praktiline soovitus
7. Suure südame-veresoonkonnahaiguste riskiga 40–65-aastase inimese LDL-kolesterooli ravieesmärk on ˂ 1,8 mmol/L ja LDL-kolesterooli sisalduse vähenemine 50% või enam algsest LDL-kolesterooli väärtusest.
Praktiline soovitus
2. tüüpi diabeedi varane avastamine
8. 40–65-aastasele 2. tüüpi diabeedi riskiga inimesele võite määrata paastuglükoosi või glükohemoglobiini analüüsi haiguse varaseks avastamiseks.
Nõrk positiivne soovitus, madal tõendatuse aste
PSA-analüüs eesnäärmevähi varaseks avastamiseks
9. 40–54-aastasel mehel hinnake enne PSA-analüüsi tegemist järgmiste eesnäärmevähi riskitegurite esinemist:
• eesnäärmevähi esinemine esimese astme sugulasel,
• rinnavähi esinemine esimese astme sugulasel,
• Aafrika päritolu.Nõrk positiivne soovitus, madal tõendatuse aste
10. 40–54-aastasele mehele, kellel esineb vähemalt üks eesnäärmevähi riskitegur, võite soovitada PSA-analüüsi tegemist. Teavitage meest uuringu tulemusega seotud kasust ja kahjust.
Nõrk positiivne soovitus, madal tõendatuse aste
11. 55–65-aastasele mehele võite soovitada PSA-analüüsi tegemist. Teavitage meest uuringu tulemusega seotud kasust ja kahjust.
Nõrk positiivne soovitus, madal tõendatuse aste
12. Lähtuge PSA-analüüside tõlgendamisel ja järgmise kontrolli vajaduse hindamisel ravijuhendi tabelist 3.
Praktiline soovitus
Glaukoomi varane avastamine
13. 40–65-aastaselt inimeselt küsige, kas kellelgi tema esimese astme sugulastest on esinenud glaukoom.
Nõrk positiivne soovitus, väga madal tõendatuse aste
14. 40–65-aastane inimene, kelle esimese astme sugulasel on diagnoositud glaukoom, suunake oftalmoloogi vastuvõtule.
Praktiline soovitus
Osteoporoosi varane avastamine
15. 40–65-aastasel naisel võite osteoporoosi riski hindamiseks kasutada luumurruriski kalkulaatorit FRAX.
Nõrk positiivne soovitus, väga madal tõendatuse aste
16. 40–65-aastane naine suunake luudensitomeetria uuringule, kui luumurruriski kalkulaatori FRAX järgi on kümne aasta reieluukaela murru risk ≥ 2% ja üldine luumurru risk ≥ 6%.
Praktiline soovitus
17. 40–65-aastast naist nõustage osteoporoosi riskitegurite suhtes.
Praktiline soovitus
D-vitamiini lisamanustamine ja sisalduse määramine verest
18. Kui on kahtlus, et inimene ei saa toidust piisavalt D-vitamiini, nõustage teda tervisliku toitumise teemal, lähtudes Eesti toitumis- ja liikumissoovitustest.
Praktiline soovitus
19. Tubase eluviisiga inimest nõustage füüsilise aktiivsuse ja õues viibimise teemal.
Praktiline soovitus
20. 40–65-aastasele inimesele võite soovitada D-vitamiini lisamanustamist 10–25 µg/päevas (400–1000 RÜ), kui tekib kahtlus, et inimene ei saa piisavalt D-vitamiini.
Nõrk positiivne soovitus, madal tõendatuse aste
21. D-hüpovitaminoosi kahtluseta 40–65-aastasel inimesel pigem ärge määrake D-vitamiini sisaldust veres.
Praktiline soovitus
Depressiooni ja ärevushäire varane avastamine
22. 40–65-aastasel inimesel kasutage depressiooni esmaseks hindamiseks küsimustikke PHQ-2 või EEK-2.
Tugev positiivne soovitus, mõõdukas tõendatuse aste
23. 40–65-aastasel inimesel võite kasutada ärevushäire esmaseks hindamiseks küsimustikke GAD-2 või EEK-2.
Nõrk positiivne soovitus, madal tõendatuse aste
Tervislike eluviiside soovitused
Kehaline aktiivsus
24. 40–65-aastaselt inimeselt küsige,
• mitmel päeval nädalas on ta kehaliselt aktiivne,
• millise intensiivsusega on tema kehaline aktiivsus,
• mitu minutit korraga on ta kehaliselt aktiivne.Vajaduse korral nõustage teda (vt lisa 5).
Praktiline soovitus
Toitumine
25. 40–65-aastaselt inimeselt küsige toitumise kohta ja uurige, milline osakaal on tema menüüs järgmistel toiduainetel:
• küllastumata rasvhappeid sisaldavad toidud (rasvane kala, pähklid ja seemned, avokaado, oliivid, taimeõli);
• kiudainerikkad taimsed toidud (köögiviljad, täisteratooted, kaunviljad, puuviljad ja marjad);
• punane ja töödeldud liha (võrreldes kala, linnuliha ja munaga);
• lisatud suhkur (nt suhkruga karastusjoogid), ohtralt suhkruid ja rasvu sisaldavad toidud (nt maitsestatud jogurtid);
• sool.Vajaduse korral nõustage teda (vt lisa 5).
Praktiline soovitus
Tubaka- või nikotiinitoodete tarvitamine
26. 40–65-aastaselt inimeselt küsige tubaka- ja nikotiinitoodete tarvitamise kohta. Kui ta tarvitab mainitud tooteid, siis nõustage teda ravijuhendi „Tubaka- või nikotiinitoodetest loobumise nõustamine“ põhjal.
Praktiline soovitus
Alkoholitarvitamine
27. 40–65-aastase inimese alkoholitarvitamise hindamiseks kasutage AUDIT-testi. Alkoholi liigtarvitamise kahtluse korral (skoor ≥ 8 punkti) tehke lühisekkumine ja edasisel käsitlusel lähtuge ravijuhendist „Alkoholitarvitamise häirega patsiendi käsitlus“.
Praktiline soovitus
Narkootiliste ainete tarvitamine
28. 40–65-aastaselt inimeselt küsige narkootiliste ainete tarvitamise kohta.
Praktiline soovitus
Immuniseerimine
29. 40–65-aastase inimese immuniseerimise vajaduse hindamisel lähtuge Terviseameti täiskasvanute vaktsineerimise juhistest.
Praktiline soovitus
Vähi sõeluuringud
30. 40–65-aastasele inimesele soovitage sõeluuringutes osalemist riikliku sõeluuringute korralduse alusel.
Praktiline soovitus
HIV-testimine
31. Soovitage kord aastas HIV-testimist 40–65-aastasele inimesele, kes kuulub riskirühma*, või isikule, kel on diagnoositud HIV-iga seotud indikaatorseisund(id), aga kellel ei ole positiivset HIV-testi tulemust ega diagnoositud HIVinfektsiooni.
Praktiline soovitus
* Riskirühma kuuluvad narkootikume süstivad või süstinud inimesed, prostitutsiooni kaasatud inimesed, meestega seksivad mehed, nimetatud inimeste sekspartnerid, inimesed, kellel on olnud vahekord HIV-positiivse inimesega, inimesed, kellel on olnud mitu juhupartnerit ja kaitsmata vahekord.
- Avaldumus (ingl incidence) – Näitaja, mis väljendab uute juhtude teket algselt tulemivabas rahvastikus kindlal ajavahemikul
- Glükohemoglobiin (HbA1c, ingl glycated hemoglobin) – Glükeeritud hemoglobiin ehk glükohemoglobiin moodustub, kui hemoglobiini aminorühmale lisatakse suhkrujääk. Glükohemoglobiini hulk veres on võrdelises sõltuvuses vere glükoosisisaldusega ja on mõjutatud punaste vererakkude ehk erütrotsüütide elueast.
- Glükoositaluvuse häire (ingl impaired glucose tolerance, IGT) – Seisund, mille puhul on glükoositaluvuse proovi alusel vere paastuglükoosi sisaldus < 7,0 mmol/L ja glükoosisisaldus kaks tundi pärast glükoosilahuse joomist vahemikus ≥ 7,8 ja < 11,1 mmol/L
- Glükoositaluvuse proov (ingl glucose tolerance test, GTT) Test glükoosi ainevahetushäire tuvastamiseks. Uuringu alus on glükoosi kontsentratsioon paastuplasmas ja selle muutus kaks tundi pärast 75 grammi glükoosi manustamist.
- Haigestumus (ingl morbidity) – Üldmõiste, millega kirjeldatakse haigusjuhtude esinemist või teket mingis rahvastikus
- Paastuglükoosi analüüs – Glükoosi ainevahetushäire tuvastamise analüüs, mis näitab glükoosisisaldust paastuplasmas
- Paastuglükoosi häire (ingl impaired fasting glucose, IFG) – Seisund, mille puhul on glükoositaluvuse proovi alusel vere paastuglükoosi sisaldus 6,1–6,9 mmol/L ja glükoosisisaldus kaks tundi pärast glükoosilahuse joomist < 7,8 mmol/L
- PSA-analüüs (ingl prostate-specific antigen test) – Eesnäärme- ehk prostataspetsiifilise antigeeni analüüs. Prostataspetsiifiline antigeen on valk, mida toodavad eesnäärme normaalsed rakud ja vähirakud. Antigeeni sisaldust on võimalik määrata vereanalüüsiga, et hinnata eesnäärme patoloogia olemasolu.
- Võimalusepõhine ehk oportunistlik ennetus – Ennetusviis, mille puhul ei kutsuta kõiki sihtrühma kuuluvaid inimesi aktiivselt visiidile, vaid kaasatakse ennetusse mingi varem tuvastatud riskiteguri alusel, isiku soovil või mõnel muul tingimusel.
- Mitte-HDL-kolesterool (ingl non-high-density lipoproteins cholesterol) Mitte-HDL-kolesterooli kasutatakse südame-veresoonkonnahaiguste riski hindamiseks, sh riskiskooris SCORE2. Teatud juhtudel peegeldab see riski paremini kui LDL-kolesterool. Mitte-HDL-kolesterooli väärtuse saamiseks lahutatakse üldkolesteroolist HDL-kolesterool.
- Narkootilised ained – Narkootilised ja psühhotroopsed ained on meeleolu ja käitumist mõjutavad ained, millel võib olla valuvaigistav toime ning millega kaasneb suur sõltuvuse oht.
1. Pruks L-L, , Alloja J, , Suurna M, , Rätsep A, , Laisaar K-T, , Kiivet R, , Jürisson M, . Tervisekontrollid südame-veresoonkonnahaiguste ja diabeedi ennetuseks, TTH56. Tartu Ülikooli peremeditsiini ja rahvatervishoiu instituut; 2022.
2. Estonian Health Insurance Fund, . Estonian Handbook of Guidelines Development 2020. Tallinn: Estonian Health Insurance Fund; 2021.
3. Visseren FLJ, Mach F,Smulders YM,et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J; 2021.
4. SCORE2 working group, ESC Cardiovascular risk collaboration. SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe. Eur Heart J; 2021.
5. Ferraz-Amaro I, Corrales A,Atienza-Mateo B,et al. SCORE2 Assessment in the Calculation of Cardiovascular Risk in Patients with Rheumatoid Arthritis. Diagnostics (Basel); 2021.
6. Mach, F, Baigent, C, Catapano, AL,, et al, . 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk: The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). European Heart Journal; 2020.
7. Ference, BA, Ginsberg, HN, Graham , I, et al, . Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J; 2017.
8. Cholesterol Treatment Trialists Collaboration, , Baigent, C, Blackwell, L, et al, . Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet; 2010.
9. Taylor F, Human MD,Macedo AF,Moore THM,Burke M,Davey Smith G,Ward K,Ebrahim S,Gay HC.. Statins for the primary prevention of cardiovascular disease. Cochrane Database of Systematic Reviews; 2013.
10. Sandwith, L., Forget, P.. Statins in Healthy Adults: A Meta-Analysis.. Medicina; 2021.
11. Chou R, Dana T,Blazina I,Daeges M,Jeanne TL.. Statins for Prevention of Cardiovascular Disease in Adults: Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA; 2016.
12. Cholesterol Treatment Trialists’ (CTT) Collaborators,, , Mihaylova, B, Emberson, J, et al, . The effects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomised trials. Lancet; 2012.
13. Cholesterol Treatment Trialists Collaboration, , Fulcher, J, O’Connell, R, et al, . Efficacy and safety of LDL-lowering therapy among men and women: meta-analysis of individual data from 174,000 participants in 27 randomised trials. Lancet; 2015.
14. Wang, N, Fulcher, J, Abeysuriya , N, et al, . Intensive LDL cholesterol-lowering treatment beyond current recommendations for the prevention of major vascular events: a systematic review and meta-analysis of randomised trials including 327 037 participants. Lancet Diabetes Endocrinol; 2020.
15. Stone , NJ, Robinson , JG, Lichtenstein , AH, et al, . Very low levels of atherogenic lipoproteins and the risk for cardiovascular events: a meta-analysis of statin trials. J Am Coll Cardiol; 2014.
16. Vallejo-Vaz, AJ, Robertson , M, Catapano , AL. Low-density lipoprotein cholesterol lowering for the primary prevention of cardiovascular disease among men with primary elevations of low-density lipoprotein cholesterol levels of 190 mg/dL or above: analyses from the WOSCOPS (West of Scotland Coronary Prevention Study) 5-year randomized trial and 20-year observational follow-up.. Circulation; 2017.
17. Ravijuhendite nõukoda, . Täiskasvanute kõrgvererõhktõve käsitlus esmatasandil, RJ-I/1.2-2019. 2019.
18. Brugts, JJ, Yetgin, T, Hoeks , SE, et al, . The benefits of statins in people without established cardiovascular disease but with cardiovascular risk factors: meta-analysis of randomised controlled trials. BMJ; 2009.
19. Mills, EJ, Rachlis, B, Wu, P, et al, . Primary prevention of cardiovascular mortality and events with statin treatments: a network metaanalysis involving more than 65,000 patients. 52; 2008.
20. Tervise Arengu Instituut, . Diabeedi esmashaigestumus on Eestis langustrendis. Uudised; 2021.
21. Hoyer A, Rathmann W Kuss O. Utility of HbA1c and fasting plasma glucose for screening of Type 2 diabetes: a meta-analysis of full ROC curves. Diabet Med; 2018.
22. Chivese T, Hirst J,Matizanadzo JT,Custodio M,Farmer A,Norris S,Levitt N. The diagnostic accuracy of HbA1c, compared to the oral glucose tolerance test, for screening for type 2 diabetes mellitus in Africa-A systematic review and meta-analysis. Diabet Med.; 2022.
23. Kodama S, Horikawa C,Fujihara K,Hirasawa R,Yachi Y,Yoshizawa S,Tanaka S,Sone Y,Shimano H,Iida KT,Saito K,Sone H. Use of high-normal levels of haemoglobin A(1C) and fasting plasma glucose for diabetes screening and for prediction: a meta-analysis. Diabetes Metab Res Rev; 2013.
24. Kaur G, Lakshmi PVM,Rastogi A,Bhansali A,Jain S,Teerawattananon Y,Bano H,Prinja S. Diagnostic accuracy of tests for type 2 diabetes and prediabetes: A systematic review and meta-analysis. PLoS One; 2020.
25. Barry E, Roberts S,Oke J,Vijayaraghavan S,Normansell R,Greenhalgh T.. Efficacy and effectiveness of screen and treat policies in prevention of type 2 diabetes: systematic review and meta-analysis of screening tests and interventions. BMJ; 2017.
26. Lee CMY, Colagiuri S,Woodward M,Gregg EW,Adams R,Azizi F,Gabriel R,Gill TK,Gonzalez C,Hodge A,Jacobs Jr DR Jr,Joseph JJ,Khalili D,Magliano DJ,Mehlig K,Milne R,Mishra G,Mongraw-Chaffin M,Pasco JA,Sakurai M,Schreiner PJ,Selvin E,Shaw JE,Wittert G,Yatsuya H,Huxley RR. Comparing different definitions of prediabetes with subsequent risk of diabetes: an individual participant data meta-analysis involving 76 513 individuals and 8208 cases of incident diabetes. BMJ Open Diabetes Res Care; 2019.
27. Bennett CM, Guo M,Dharmage SC. HbA(1c) as a screening tool for detection of Type 2 diabetes: a systematic review. Diabet Med; 2007.
28. American Diabetes Association, . Standards of Medical Care in Diabetes – 2021.. Diabetes Care; 2021.
29. , . 2. tüüpi diabeedi diagnostika ja ravi. Ravijuhend. RJ-E/51.1-2021. Eesti Haigekassa; 2021.
30. Tervise Arengu Instituut, . Tervisestatistika ja terviseuuringute andmebaas, PK10: Pahaloomuliste kasvajate esmasjuhud paikme, soo ja vanuserühma järgi, kasutatud 10.02.2023.
31. Tervise Arengu Instituut, . ervisestatistika ja terviseuuringute andmebaas, SD21: Surmad põhjuse, soo ja vanuserühma järgi, kasutatud 10.02.2023.
32. Jürisson, M, Alloja , J, Punab , M, et al, . Organiseeritud sõeluuring eesnäärmevähi varaseks diagnoosimiseks Eestis: tervisetehnoloogia hindamise raport TTH26. Tartu Ülikooli peremeditsiini ja rahvatervishoiu instituut; 2017.
33. Veskimäe P, Žarkovski M Kivi M Kiivet R. Eesnäärmevähi varane avastamine. TTH49. Tartu Ülikooli peremeditsiini ja rahvatervishoiu instituut; 2020.
34. RACGP, . The Royal Australian College of General Practitioners. Guidelines for preventive activities in general practice. 9th edn. East Melbourne, Vic; 2016.
35. US Preventive Services Task Force, Grossman DC,Curry SJ,et al. Screening for Prostate Cancer: US Preventive Services Task Force Recommendation Statement. JAMA; 2018.
36. National Comprehensive Cancer Network, . NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Prostate Cancer Early Detection. Version 2.2021.. 2021.
37. Tikkinen KAO, Dahm P,Lytvyn L,et al. Prostate cancer screening with prostate-specific antigen (PSA) test: a clinical practice guideline. BMJ; 2018.
38. Mottet N, Cornford P,van den Bergh RCN,et al. EAU-EANM-ESTRO-ESUR-SIOG Guidelines on Prostate Cancer. EAU Guidelines. Edn. presented at the EAU Annual Congress Milan 2021.. EAU; 2021.
39. Punab M, Takker U,Palts K,et al. Meeste kusemishäirete käsitlus- ja ravijuhend perearstidele. Eesti Arst; 2011.
40. Ilic D, Djulbegovic M Jung JH et al. Prostate cancer screening with prostate-specific antigen (PSA) test: a systematic review and meta-analysis. BMJ; 2018.
41. Hugosson J, Roobol MJ,Månsson M,et al. A 16-yr Follow-up of the European Randomized study of Screening for Prostate Cancer. Eur Urol; 2019.
42. Martin RM, Donovan JL,Turner EL,et al. Effect of a Low-Intensity PSA-Based Screening Intervention on Prostate Cancer Mortality: The CAP Randomized Clinical Trial. JAMA; 2018.
43. Pinsky PF, Miller E,Prorok P,et al. Extended follow-up for prostate cancer incidence and mortality among participants in the Prostate, Lung, Colorectal and Ovarian randomized cancer screening trial. BJU Int; 2019.
44. Pashen U, Sturtz S,Fleer D,et al. Assessment of prostate-specific antigen screening: an evidence-based report by the German Institute for Quality and Efficiency in Health Care. BJU Int; 2022.
45. Ilic D, Neuberger MM,Djulbegovic M,et al. Screening for prostate cancer. Cochrane Database Syst Rev; 2013.
46. Randazzo M, Müller A,Carlsson S,et al. A positive family history as a risk factor for prostate cancer in a population-based study with organised prostate-specific antigen screening: results of the Swiss European Randomised Study of Screening for Prostate Cancer (ERSPC, Aarau). BJU Int; 2016.
47. Barber L, Gerke T,Markt SC,et al. Family history of breast or prostate cancer and prostate cancer risk. Clin Cancer Res; 2018.
48. Beebe-Dimmer JL, Kapron AL,Fraser AM,et al. Risk of Prostate Cancer Associated With Familial and Hereditary Cancer Syndromes. J Clin Oncol; 2020.
49. Urabe F, Kimura S,Yamamoto S,et al. Impact of family history on oncological outcomes in primary therapy for localized prostate cancer patients: a systematic review and meta-analysis. Prostate Cancer Prostatic Dis; 2021.
50. Zeegers MPA, Jellema A,Ostrer H. Empiric risk of prostate carcinoma for relatives of patients with prostate carcinoma: a meta-analysis. Cancer; 2003.
51. Ren ZJ, Cao DH,Zhang Q,et al. First-degree family history of breast cancer is associated with prostate cancer risk: a systematic review and meta-analysis. BMC Cancer; 2019.
52. Miller EA, Pinsky PF,Black A,et al. Secondary prostate cancer screening outcomes by race in the Prostate, Lung, Colorectal, and Ovarian (PLCO) Screening Trial. Prostate; 2018.
53. Crosswell JM, Kramer BS,Kreimer AR,et al. Cumulative Incidence of False-Positive Results in Repeated, Multimodal Cancer Screening. Ann Fam Med; 2009.
54. Kilpeläinen TP, Tammela TL,Roobol M,et al. False-positive screening results in the European randomized study of screening for prostate cancer. Eur J Cancer; 2011.
55. Vernooij RWM, Lytvyn L,Pardo-Hernandez H,et al. Values and preferences of men for undergoing prostate-specific antigen screening for prostate cancer: a systematic review. BMJ Open; 2018.
56. USPSTF, . Screening for Primary Open-Angle Glaucoma: US Preventive Services Task Force Recommendation Statement. JAMA; 2022.
57. AAO, . Primary Open-Angle Glaucoma Preferred Practice Pattern. 2020.
58. Chou R, Selph S,Blazina I,Bougatsos C,Jungbauer R,Fu R,Grusing S,Jonas DE,Tehrani S. Screening for Glaucoma in Adults: Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA; 2022.
59. Swamy B, Cumming RG,Ivers R,et al. Vision screening for frail older people: a randomised trial. Br J Ophthalmol; 2009.
60. Hollands H, Johnson D,Hollands S,Simel DL,Jinapriya D,Sharma S. Do findings on routine examination identify patients at risk for primary open-angle glaucoma? The rational clinical examination systematic review. JAMA; 2013.
61. SIGN, Scottish Intercollegiate Guidelines Network. Management of osteoporosis and the prevention of fragility fractures.. SIGN; 2021.
62. USPSTF, . Screening for Osteoporosis to Prevent Fractures US Preventive Services Task Force Recommendation Statement. JAMA; 2018.
63. Viswanathan M, Reddy S,Berkman N,et al. Screening to Prevent Osteoporotic Fractures: Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA; 2018.
64. Shepstone L, Lenaghan E Cooper C et al. SCOOP Study Team. Screening in the community to reduce fractures in older women (SCOOP): a randomised controlled trial. Lancet; 2017.
65. Hippisley-Cox J, Coupland C. Predicting risk of osteoporotic fracture in men and women in England and Wales: prospective derivation and validation of QFractureScores. BMJ; 2009.
66. Drake MT, Murad MH,Mauck KF,Lane MA,Undavalli C,Elraiyah T,Stuart LM,Prasad C,Shahrour A,Mullan RJ,Hazem A,Erwin PJ,Montori VM. Clinical review. Risk factors for low bone mass-related fractures in men: a systematic review and meta-analysis. J Clin Endocrinol Metab; 2012.
67. Anagnostis P, Siolos P,Gkekas NK,Kosmidou N,Artzouchaltzi AM,Christou K,Paschou SA,Potoupnis M,Kenanidis E,Tsiridis E,Lambrinoudaki I,Stevenson JC,Goulis DG. Association between age at menopause and fracture risk: a systematic review and meta-analysis. Endocrine. Endocrine; 2019.
68. Kanis JA, Johansson H,Oden A,Johnell O,De Laet C,Eisman JA,McCloskey EV,Mellstrom D,Melton LJ 3rd,Pols HA,Reeve J,Silman AJ,Tenenhouse A. A family history of fracture and fracture risk: a meta-analysis. Bone; 2004.
69. Kanis JA, Johnell O,De Laet C,Johansson H,Oden A,Delmas P,Eisman J,Fujiwara S,Garnero P,Kroger H,McCloskey EV,Mellstrom D,Melton LJ,Pols H,Reeve J,Silman A,Tenenhouse A. A meta-analysis of previous fracture and subsequent fracture risk. Bone; 2004.
70. Hippisley-Cox J, Coupland C. Derivation and validation of updated QFracture algorithm to predict risk of osteoporotic fracture in primary care in the United Kingdom: prospective open cohort study.. BMJ; 2012.
71. Bow CH, Cheung E,Cheung CL,Xiao SM,Loong C,Soong C,Tan KC,Luckey MM,Cauley JA,Fujiwara S,Kung AW. Ethnic difference of clinical vertebral fracture risk. Osteoporos Int; 2012.
72. Mortensen SJ, Mohamadi A,Wright CL,Chan JJ,Weaver MJ,von Keudell A,Nazarian A. Medications as a Risk Factor for Fragility Hip Fractures: A Systematic Review and Meta-analysis. Calcif Tissue Int; 2020.
73. Mortensen SJ, Beeram I Florance J Momenzadeh K Mohamadi A Rodriguez EK von Keudell A Nazarian A.. Modifiable lifestyle factors associated with fragility hip fracture: a systematic review and meta-analysis. J Bone Miner Metab; 2021.
74. Godos J, Giampieri F,Chisari E,Micek A,Paladino N,Forbes-Hernández TY,Quiles JL,Battino M,La Vignera S,Musumeci G,Grosso G. Alcohol Consumption, Bone Mineral Density, and Risk of Osteoporotic Fractures: A Dose-Response Meta-Analysis. Int J Environ Res Public Health; 2022.
75. Cheraghi Z, Doosti-Irani A,Almasi-Hashiani A,Baigi V,Mansournia N,Etminan M,Mansournia MA. The effect of alcohol on osteoporosis: A systematic review and meta-analysis. Drug Alcohol Depend; 2019.
76. Kanis JA, , Cooper C, , Rizzoli R, , Reginster JY, , Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis (ESCEO) and the Committees of Scientific Advisors and National Societies of the International Osteoporosis Foundation (IOF), . European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int; 2019.
77. Pitsi T, Zilmer M,Vaask S,et al. Eesti toitumis- ja liikumissoovitused 2015. Tervise Arengu Instituut; 2017.
78. Yao P, Bennett D,Mafham M,et al. Vitamin D and Calcium for the Prevention of Fracture: A Systematic Review and Meta-analysis. JAMA Netw Open; 2019.
79. Zheng Y, Zhu J,Zhou M,et al. Meta-analysis of long-term vitamin D supplementation on overall mortality. PLoS One; 2013.
80. Zhao JG, Zeng XT,Wang J,Liu L. Association Between Calcium or Vitamin D Supplementation and Fracture Incidence in Community-Dwelling Older Adults: A Systematic Review and Meta-analysis. JAMA; 2017.
81. Bjelakovic G, Gluud LL,Nikolova D et al. Vitamin D supplementation for prevention of mortality in adults. Cochrane Database Syst Rev; 2014.
82. Li S, Xi C,Li L et al. Comparisons of different vitamin D supplementation for prevention of osteoporotic fractures: a Bayesian network meta-analysis and meta-regression of randomised controlled trials. Int J Food Sci Nutr; 2021.
83. Kahwati LC, Weber RP,Pan H,et al. Vitamin D, Calcium, or Combined Supplementation for the Primary Prevention of Fractures in Community-Dwelling Adults: Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA; 2018.
84. Kahwati LC, LeBlanc E,Weber RP,et al. Screening for Vitamin D Deficiency in Adults Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA; 2021.
85. Cashman KD, , Ritz C,, , Kiely M, , Odin Collaborators, . Improved Dietary Guidelines for Vitamin D: Application of Individual Participant Data (IPD)-Level Meta-Regression Analyses. Nutrients; 2017.
86. NICE, . Vitamin D: supplement use in specific population groups. 2014.
87. Organization, World,Health. Depression and other common mental disorders: global health estimates. Geneva: World Health Organization; 2017.
88. Instituut, Tervise,Arengu. Tervisestatistika ja terviseuuringute andmebaas. Tervisekäitumine ja tervis.
89. Jackson JL, Machen JL. From the Editors’ Desk: The Importance of Screening for Depression in Primary Care. J gen intern med; 2020.
90. Ööpik P, Aluoja A,Kalda R,Maaroos H. Screening for depression in primary care. Family Practice; 2006.
91. Tsoi KK, Chan JY,Hirai HW,Wong SY. Comparison of diagnostic performance of Two-Question Screen and 15 depression screening instruments for older adults: systematic review and meta-analysis. Br J Psychiatry; 2017.
92. Mitchell AJ, Coyne JC. Do ultra-short screening instruments accurately detect depression in primary care? A pooled analysis and meta-analysis of 22 studies. Br J Gen Pract; 2007.
93. Bosanquet K, Bailey D,Gilbody S,Harden M,Manea L,Nutbrown S,McMillan D. Diagnostic accuracy of the Whooley questions for the identification of depression: a diagnostic meta-analysis. BMJ Open; 2015 .
94. Levis B, Sun Y,He C,et al. Accuracy of the PHQ-2 Alone and in Combination With the PHQ-9 for Screening to Detect Major Depression: Systematic Review and Meta-analysis. . JAMA; 2020.
95. Manea L, Gilbody S,Hewitt C,North A,Plummer F,Richardson R,Thombs BD,Williams B,McMillan D.. Identifying depression with the PHQ-2: A diagnostic meta-analysis.. J Affect Disord; 2016.
96. El-Den S, Chen TF,Gan YL,Wong E,O’Reilly CL.. The psychometric properties of depression screening tools in primary healthcare settings: A systematic review.. J Affect Disord; 2018.
97. Wu Y, Levis B,Sun Y,He C,Krishnan A,Neupane D,Bhandari PM,Negeri Z,Benedetti A,Thombs BD,DEPRESsion Screening Data (DEPRESSD) HADS Group. Accuracy of the Hospital Anxiety and Depression Scale Depression subscale (HADS-D) to screen for major depression: systematic review and individual participant data meta-analysis. BMJ; 2021.
98. He C, Levis B,Riehm KE,Saadat N,Levis AW,Azar M,Rice DB,Krishnan A,Wu Y,Sun Y,Imran M,Boruff J,Cuijpers P,Gilbody S,Ioannidis JPA,Kloda LA,McMillan D,Patten SB,Shrier I,Ziegelstein RC,Akena DH,Arroll B,Ayalon L,Baradaran HR,Baron M,Beraldi A,Bombardier CH,Butterworth P,Carter G,Chagas MHN,Chan JCN,Cholera R,Clover K,Conwell Y,de Man-van Ginkel JM,Fann JR,Fischer FH,Fung D,Gelaye B,Goodyear-Smith F,Greeno CG,Hall BJ,Harrison PA,Härter M,Hegerl U,Hides L,Hobfoll SE,Hudson M,Hyphantis TN,Inagaki M,Ismail K,Jetté N,Khamseh ME,Kiely KM,Kwan Y,Lamers F,Liu SI,Lotrakul M,Loureiro SR,Löwe B,Marsh L,McGuire A,Mohd-Sidik S,Munhoz TN,Muramatsu K,Osório FL,Patel V,Pence BW,Persoons P,Picardi A,Reuter K,Rooney AG,da Silva Dos Santos IS,Shaaban J,Sidebottom A,Simning A,Stafford L,Sung S,Tan PLL,Turner A,van Weert HCPM,White J,Whooley MA,Winkley K,Yamada M,Thombs BD,Benedetti A. The Accuracy of the Patient Health Questionnaire-9 Algorithm for Screening to Detect Major Depression: An Individual Participant Data Meta-Analysis. Psychother Psychosom; 2020.
99. Moriarty AS, Gilbody S,McMillan D,Manea L. Screening and case finding for major depressive disorder using the Patient Health Questionnaire (PHQ-9): a meta-analysis. Gen Hosp Psychiatry; 2015.
100. Park SH, Lee H. Is the center for epidemiologic studies depression scale as useful as the geriatric depression scale in screening for late-life depression? A systematic review. J Affect Disord; 2021.
101. Negeri ZF, Levis B,Sun Y,He C,Krishnan A,Wu Y,Bhandari PM,Neupane D,Brehaut E,Benedetti A,Thombs BD,Depression Screening Data (DEPRESSD) PHQ Group. Accuracy of the Patient Health Questionnaire-9 for screening to detect major depression: updated systematic review and individual participant data meta-analysis. BMJ; 2021.
102. Plummer F, Manea L,Trepel D,McMillan D. Screening for anxiety disorders with the GAD-7 and GAD-2: a systematic review and diagnostic metaanalysis. Gen Hosp Psychiatry; 2016.
103. Nelson HD, Cantor A,Pappas M,Weeks C. Screening for Anxiety in Adolescent and Adult Women: A Systematic Review for the Women’s Preventive Services Initiative. Ann Intern Med; 2020.
104. Mughal AY, Devadas J,Ardman E,Levis B,Go VF,Gaynes BN. A systematic review of validated screening tools for anxiety disorders and PTSD in low to middle income countries. BMC Psychiatry; 2020.
105. , . Depressiooni ravijuhend perearstidele. Eesti Arst; 2011.
106. , . Generaliseerunud ärevushäire ja paanikahäire (agorafoobiaga või ilma) käsitlus perearstiabis. Ravijuhend. RJ-F/2.2-2020.. Eesti Haigekassa; 2021.
107. , . HIV-testimise ravijuhend. Eesti Haigekassa; 2021.
PS!
Ravijuhendi dokumente (protokollid, huvide deklaratsioone, käsitlusala, rakenduskava jms leiab Tervisekassa veebilehelt Ravijuhend.ee SIIN.